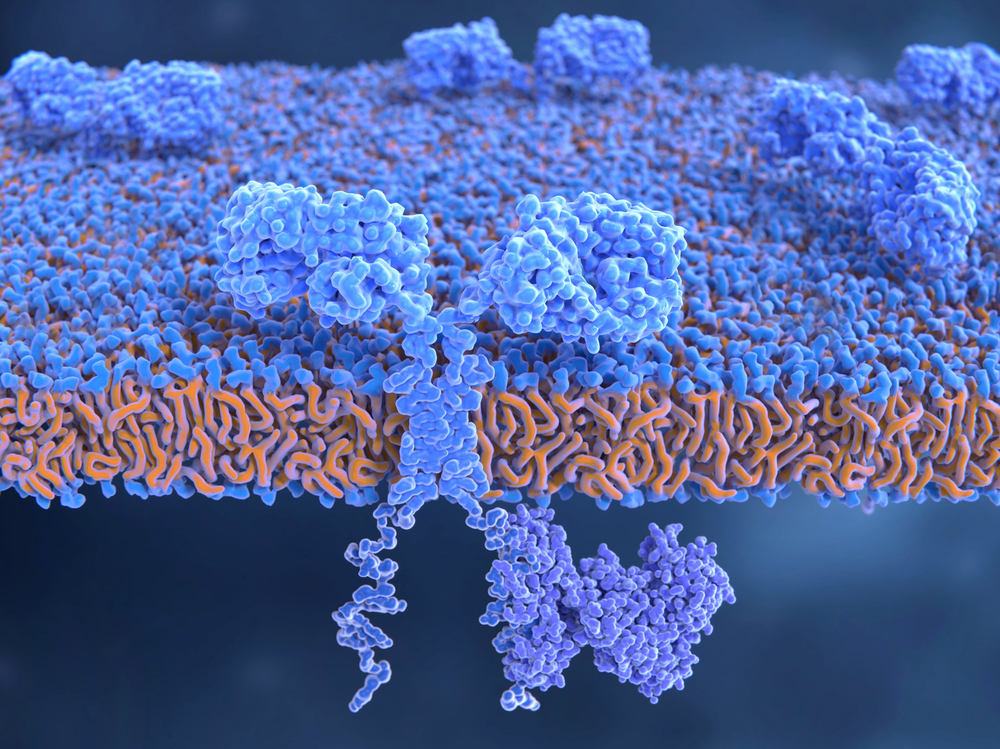
AI 引导受体工程可提高细胞疗法的性能
快速阅读: 据《基因工程和生物技术新闻》最新报道,在《基因技术》杂志上,西北大学的研究人员提出了一种基于结构的新分析方法,以改进工程受体的设计,提高细胞疗法的效果。该研究通过模型探讨了结构与功能的关系,并提出了可实验验证的设计规则。尽管结构预测工具不断进步,但仍需更多实证研究来理解受体性能,这有望加速合成受体在生物医学应用中的开发。
在《基因技术》杂志上发表的一项新研究中,题为“利用计算结构预测探索工程受体性能的结构-功能关系”,西北大学的研究人员提出了一种基于结构的新分析方法,以指导合成受体的设计,从而提高细胞疗法的效果。“一个关键挑战是细微的结构变化可能会带来显著的功能影响,因此细胞疗法可以从改进的方法中获益,这些方法能在结构层面上调节受体功能。”西北大学化学与生物工程教授、该研究的通讯作者乔舒亚·伦纳德博士在接受《基因技术》采访时说。
在细胞疗法中,工程受体需要同时具备安全性和有效性,例如保持静息状态直到遇到疾病靶点。然而,这些受体的结构通常不够明确,这可能对治疗效果产生重大影响。在CAR-T细胞疗法的例子中,结构上的调整可以避免非特异性信号传导,或在没有目标刺激的情况下激活,这常常导致T细胞衰竭,并削弱疗法对靶点(如肿瘤)的有效性。作者创建了受体结构模型,通过一个案例研究来探讨结构与功能之间的关系,该案例研究描述了将天然人类细胞因子受体转化为工程受体的过程。他们假设结构预测在基于天然受体的数据集上更为可行,因为现有工具依赖于已知蛋白质的序列比对。
研究表明,受体胞外域中的特定结构特征(通常延伸到细胞外空间以触发信号转导)和跨膜域解释了受体性能的显著差异,这是通过开启状态报告基因表达和报告基因转录水平的倍增来衡量的。作者还将分析扩展到描述特定结构选择及其组合方式的“分类”变量,这隐含地捕捉了独特的个体链特性,这些特性无法直接由结构特征描述,如蛋白质表达、膜定位、蛋白质稳定性。总体而言,他们观察到了在结构各异的受体组中普遍存在的结构-功能关系。工程受体是一类特别具有挑战性的蛋白质,需要从结构角度进行定义,因为它们相对较大,包含难以表征的疏水性跨膜域,并且可以采用多种构象。
突破性工具,如阿尔法折叠,解决了生物学标志性问题——从蛋白质序列确定其三维结构,并使德米斯·哈萨比斯博士和约翰·詹普博士分享了2024年诺贝尔化学奖;阿尔法折叠多聚体和罗斯塔折叠(由2024年诺贝尔奖获得者大卫·贝克博士开发),已经能够构建天然单次跨膜受体的完整模型。然而,提炼哪些结构特征影响受体性能依然是一个未解决的问题。“对于所有我们不理解的受体方面,我们必须投入更多时间和精力进行实证探索以确定设计选择,即使识别出好的设计,这种缺乏结构知识使得理解某些选择为何能产生良好性能更加困难。”伦纳德说。
《基因技术》研究提出了潜在的可实验验证的设计规则,可以指导未来跨受体家族的工程。伦纳德和该研究的主要作者、西北大学的博士候选人威廉·科尔科兰预计,这些见解将最直接地帮助设计具有相似信号机制的合成受体,鉴于该研究基于将天然受体(使用多种机制)转换为合成受体(使用单一机制)。展望未来,作者表示,这一工作流程的自然演进是生成探索更大设计空间的文库。此外,伦纳德的研究团队正在进行多个项目,开发并应用不同类型的合成受体,并计划将本研究的见解应用于设计新的合成受体以用于更多应用。“最终,这项研究使我们乐观地认为,尽管蛋白质结构预测工具不断改进,但它们已经可用于在受体序列和受体功能之间建立合理的联系,这一事实应该加快合成受体在众多生物医学应用中的开发进程,”科尔科兰告诉《基因技术》。
(以上内容均由Ai生成)